010-67709643
北京曼泰里生物技术有限公司
北京市朝阳区东四环中路82号3座21层2508
供者特异性抗体监测(DSA)
—— 新的临床监测指标
全球每年有超过10万例的实体器官移植,其中美国的移植数量29000例,我国的移植数量仅次于美国,尽管移植后的康复已经得到提升,理想的器官存活时间还有待提高,超过十年的肾脏器官移植尸肾和活体分别是42.7% 59.6%。 移植失败的后期主要是抗体介导的排斥起主要作用。
抗HLA抗体在移植中的作用
由于输血,妊娠,移植可以导致受者体内存在HLA抗体,HLA抗体以循环抗体的形式存在于受者体免疫系统,这导致在移植前受者是致敏的,近些年来,临床移植后监测错配的I类II类相关抗体,给移植患者带来了极大的福音。
移植前后检测出针对供者器官的抗体,如果没有给予临床治疗,就会产生免疫攻击导致移植物失功移植物丢失的危险。供者特异性抗体攻击移植物的内皮细胞,导致抗体介导的排斥。移植后DSA的产生和由相关临床事件共同导致移植物被破坏,导致慢性病理损伤最终影响移植物的功能和存活率。
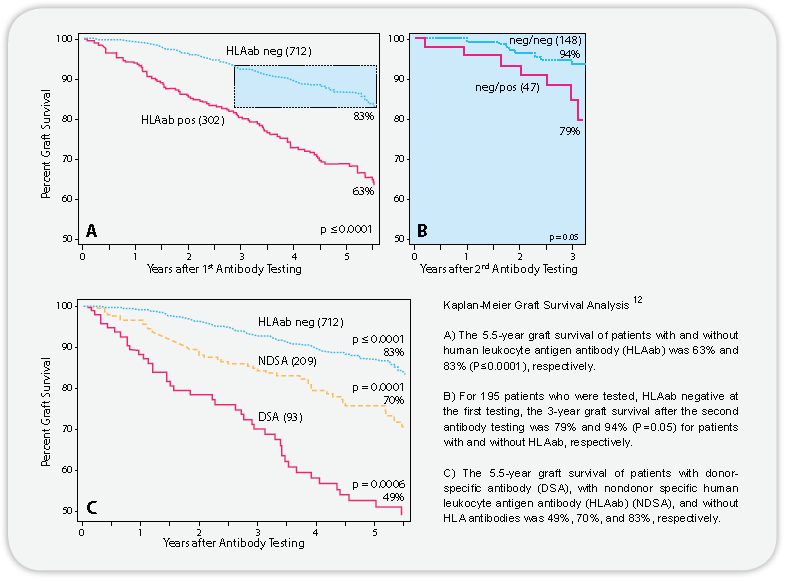
如图Kaplan-meier移植存活分析
A 肾移植患者HLA抗体阴性的移植后5.5年的存活率为83%,抗体阳性5.5年的存活率为63%(p≦0.0001)
B 监测195名肾移植患者,移植前抗体呈阴性,第二次抗体监测阳性患者3年的存活率为79%,阴性3年的存活率为94%。(p≦0.05)
C肾移植的5年半患者体内存在DSA的器官存活率为49%;NDSA为存活率70%;HLAab阴性的存活率为83%
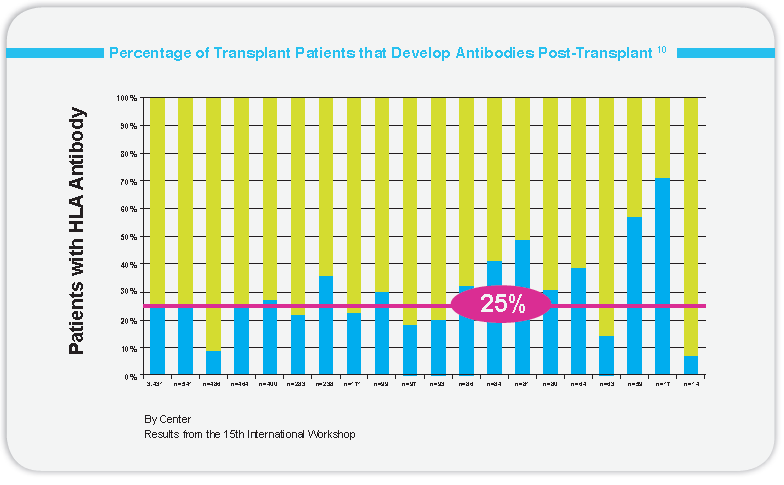
大样本量的前瞻性研究显示,在给定的时间内大约有25%的移植受者体内存有有抗体,监测DSA的肾移植的病人中,96%发生了慢性排斥。虽然传统的监测指标能够辅助诊断实体器官移植的临床状态,但是这些监测指标通常是非特异性的而且很多都发生在移植物受损之后。
这里大量的证据表明HLA抗体,能够导致慢性肾失攻,导致肾移植失败。早期诊断并在移植前后移除与抗体介导排斥相关的有害的DSA,可以阻止移植物丢失。
One lambda,Inc 提供高敏感性和特异性监测方法,在移植前后监测DSA。目前本平台在美国很多移植中心作为临床诊断标准方法。
抗体介导的排斥
抗体介导的排斥发生在早期急性阶段,常常是由记忆性反应导致,晚期或慢性阶段是由新产生的抗体导致。在急性阶段,常常是抗体导致了急性排斥。在移植后的早期,DSA的产生导致急性排斥。患者存在DSA发生抗体介导排斥几率会很高,并且会有很低的移植存活率9。
慢性排斥能够导致移植物丢失。常常被描述为郁积阶段,持续抗体介导的损伤和修复导致移植物微管系统不同的改变。患者存在DSA和新产生的DSA会增加发生慢性排斥的危险。
亚临床抗体介导的排斥
DSA的产生可能不会导致移植物的立刻失功,这类排斥,称为亚临床性排斥,据报道可能会影响长期移植物失功,而不是立即产生影响6。Loupy等研究产生DSA和亚临床排斥的患者的活组织检查,发现移植后3个月到3年,慢性病理逐渐增加,伴有持续的急性由体液引起的病变24.微循环炎症在移植后一年肾活检中更普遍,反应出高频率的DSA的产生。亚临床排斥也频繁的在产生DSA的患者的发现,其中一些亚临床排斥的患者C4d染色呈阴性。传统来讲,上述病理与不依赖免疫抑制治疗相关。
实体器官移植后受者新DSA的产生
新供者特异性抗体发展在移植后与高器官移植失败率相关10。然而一些不同的报道的患者新的DSA的百分数是不同的,从24%到62%,观察到在肝移植受者体内是最高的百分数62%。
一些新的和回忆性的研究证明在肾移植患者产生DSA,著的出现在HLAII类供者错配,与不好的结果相关,常常在移植失败是检测到。
临床获得了更透彻的理解移植后产生DSA进展的,这种现象变的非常清晰在过去误解和低估很可能由于拖延了移植后临床表现。
移植后患者产生DSA的比例 。
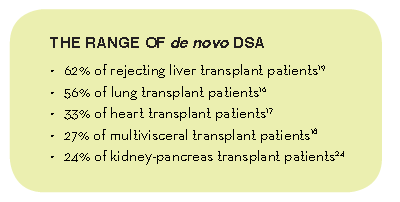
Ø 62%的肝移植排斥的患者(American Journal of Transplantation 2011; 11: 1868-1876)
Ø 56%的肺移植患者(Journal of Heart and Lung Transplantation 2010; 29:973-980)
Ø 33%的心移植患者(American Journal of Transplantation 2011; 11:312–319.)
Ø 27%的多器官移植患者(Clinical and Translational Research 2011; 92 (6): 709-715)
Ø 24%的肾移植患者(American Journal of Transplantation 2009; 9: 2561-2570)
DSA预测移植物存活率低
慢性排斥是由于持续的新的DSA的产生并且移植物失攻增加移植物丢失的危险。在肾移植受者出现II类抗体增加移植肾小球病的危险,不能长期存活。
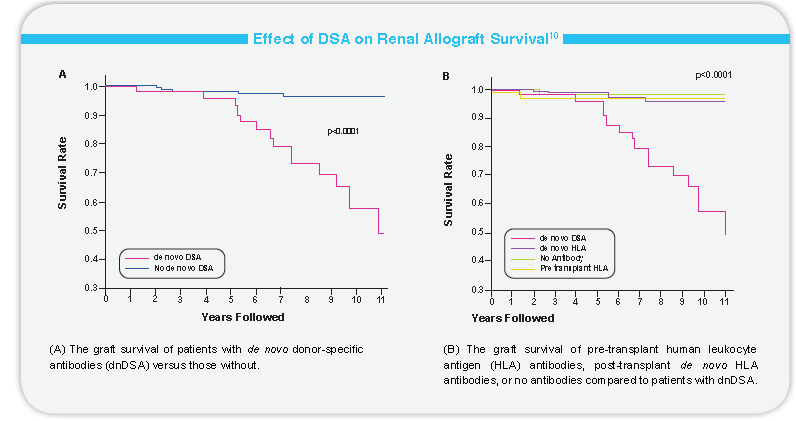
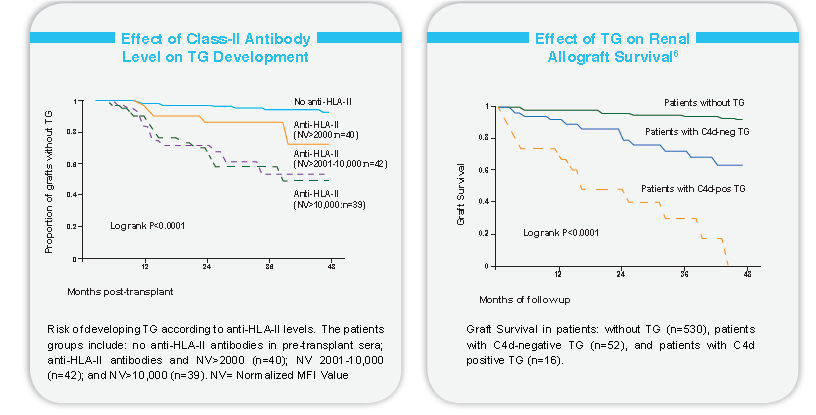
除了排斥和移植物丢失,已经证明了HLA抗体和患者的存活率存在显著地相关性,Smith等在心脏研究发现新产生的DSA能够独立预测患者的移植存活。(P<0.0001, HR =4.763)
Dunn等最新研究发现在移植后5年DSA阳性的患者与DSA阴性的患者相比存活率显著下降。(P=0.0006, HR =10.0)
肝移植
因为缺乏清晰的临床,病理学,免疫组化诊断标准,肝移植中的早期抗体介导的排斥常常很难鉴定,由于移植前没有交叉配型结果,往往被误诊为慢性移植排斥。移植时配型结果阳性,非特异性肝胆淤积的临床和病理变化与抗体介导的排斥相似,移植后患者持续性的阳性结果有发生抗体介导排斥的危险,近期数据显示肝移植中抗体介导的排斥的诊断基于是否患者血清中存在DSA。
O’Leary 等第一次证明了肝移植中DSA与慢性排斥的相关性。本组是评价了总的MFI(Mean Fluorescence Intensity),得出一类抗体比二类抗体能够更好的预测移植物的存活率。肝移植的第一年产生DSA,患者普遍伴有慢性排斥,92%的患者在慢性排斥诱发移植物丢失前检测到DSA的存在。
心脏移植
在长期心脏移植存活中,心脏移植血管病变(CAV)是最主要的引起死亡或再次移植的原因 循环抗体能够激活补体,并攻击心内皮细胞因而导致移植物失攻,引起心脏移植血管病变(CAV),使得患者死亡。
Kazmerek等研究发现,DSA阳性的患者在移植后第1年免于发生CAV的概率是94.4%,第5年是81.0%,第10年是41.2%,第15年是10.3。而DSA阴性患者分别是96.2%,83.4%,67.3%,34.7%。
移植第一年产生的抗体使得第15年的存活率为52%。
C1qDSA对移植存活率的影响
移植后监测患者的HLA抗体可以很好地预测AMR,既然不是所有的DSA都是补体依赖型的,而且这些HLA抗体不全都与器官排斥相关,那么为了更好地治疗移植病人,有必要区分是否是补体依赖型。
目前有一种新型的C1q分析方法可以检测补体依赖的IgG抗体,用于分析病人的免疫状态。近期研究发现心脏移植患者中,所有C1q阳性的患者病检时发现都发生了AMR排斥。
通过检测C4d沉积来预测抗体介导的排斥(AMR)没有被广泛的认可,因为发生C4d沉积时已经发生了AMR,并且最近研究发现C4d沉积与AMR的关联性不强,。研究表明C1q分析方法可以提供更近一步的免疫抗体筛选信息,能够提供最佳的临床检测指标。
目前C1q+DSA与急性排斥显著相关,C1q+DSA的患者在病理活检中更易发现C1d沉积。C1q分析方法能检测出能够与补体结合并激活补体的抗体。25.5%肾移植患者在移植后一年内检测出DSA的患者是C1q阳性。C1q+ DSA的患者与阴性患者在移植的第一年内发生AMR的概率分别为64.3%:13.4% 。多重分析证明移植第一年内C1q+DSA与移植物失攻有独立的相关性。(HR=6.9;CI=1.5-32.6,p=0.1)
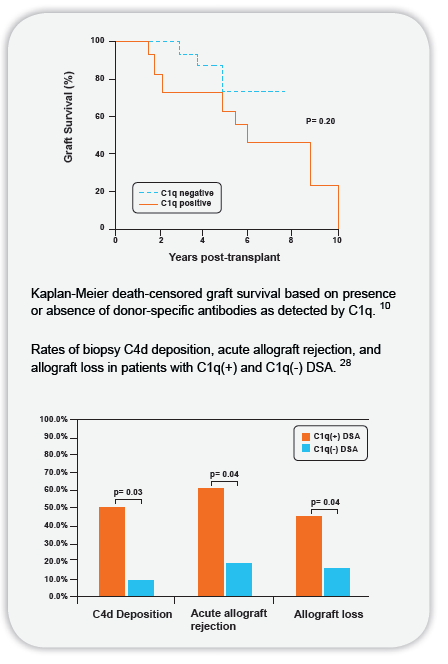
许多患者在移植前DSA为阴性,典型的在移植后2年内产生DSA。
通过病理活检和慢性移植肾病的病理症状来诊断AMR的发生,目前50%的发生AMR的患者被忽略了,抗体在几个月或者几年内诱导慢性血管病变,最终导致移植失败。
常规监测DSA能够早期预测患者是否会发生排斥的危险,。DSA的监测能够帮助移植后调整免疫治疗方案。更近的监视体液免疫是能够精确的调整抗体液治疗和最佳结果。
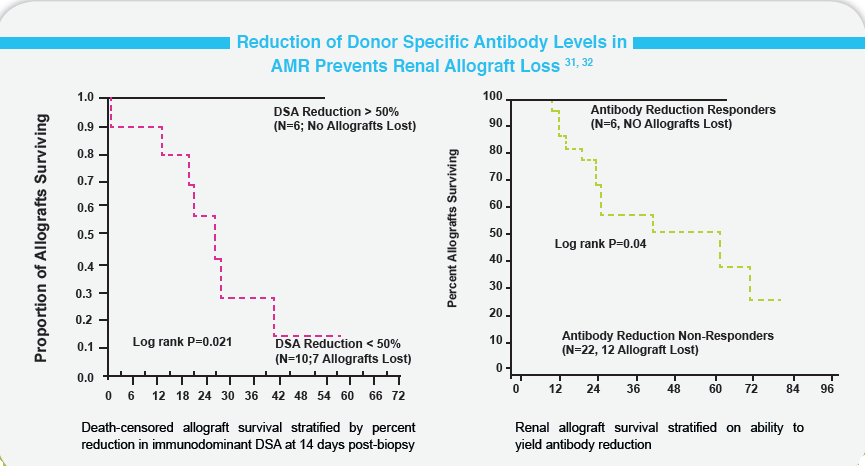
研究发现通过早期常规DSA监测,最初的抗体液治疗开始的很快,允许DSA清除和提高整体移植存活率。
在持续性的产生DSA患者中比清除DSA的患者存活率显著降低。
DSA的监测方法——单一抗原微珠监测
单一抗原微珠,应用Luminex XMAP技术,灵敏的监测移植患者的DSA 。
样本:受者和供者的全血——配型 受者的血清—抗体
检验流程:受者和供者的配型结果—
受者的抗体检测—
比对供受者抗原型别和受者单一抗体检测结果判断是否为DSA
单一抗原磁珠检测的优势
Ø 低PRA的患者检测出低水平的DSA也存在发生排斥的危险
Ø 高PRA的患者如果没有DSA,那么移植也是相对安全的。
Ø DSA的改变和新DSA的产生都揭示出早期排斥的可能
移植后常规DSA监测作为一种临床检测指标已经得到了广泛的认可,移植后监测频率根据患者的移植后发生AMR的危险性来制定的,一系列的监测结果比单一结果更能反应情况,特别是移植后的监测,是预测患者发生排斥的关键。